醫(yī)藥 · 看點(diǎn)
外用無敵膏非處方藥說明書范本修訂�����,我國自主研發(fā)的創(chuàng)新藥注射用泰它西普獲附條件批準(zhǔn)上市……3月8~14日�����,醫(yī)藥行業(yè)的這些事情值得關(guān)注。
行業(yè) · 政策動態(tài)
1.國家藥監(jiān)局發(fā)布《眼科光學(xué) 人工晶狀體 第2部分:光學(xué)性能及測試方法》等63項(xiàng)行業(yè)標(biāo)準(zhǔn)和3項(xiàng)修改單�。
2.國家藥監(jiān)局發(fā)布關(guān)于醫(yī)療器械主文檔登記事項(xiàng)的公告,該公告適用于進(jìn)口第二類����、第三類及境內(nèi)第三類醫(yī)療器械(含體外診斷試劑)注冊���、變更、臨床試驗(yàn)審批等申請事項(xiàng)中所引用主文檔的登記�。
3.國家藥監(jiān)局決定對外用無敵膏非處方藥說明書范本進(jìn)行修訂,本品的上市許可持有人應(yīng)依據(jù)有關(guān)規(guī)定����,提出修訂說明書的補(bǔ)充申請,于6月9日前報(bào)省級藥品監(jiān)督管理部門備案�����。
4.國家藥監(jiān)局藥審中心(CDE)發(fā)布《創(chuàng)新藥(化學(xué)藥)臨床試驗(yàn)期間藥學(xué)變更技術(shù)指導(dǎo)原則(試行)》《境外已上市境內(nèi)未上市化學(xué)藥品藥學(xué)研究與評價(jià)技術(shù)要求(試行)》《中藥變更受理審查指南(試行)》�����,均自發(fā)布之日起施行���。
5.CDE發(fā)布《化學(xué)仿制藥參比制劑目錄(第四十一批)》(征求意見稿)��,涉及甲磺酸奧希替尼片等藥品��,公示時(shí)間為3月12~25日�����。
產(chǎn)品研發(fā) · 上市信息
1.國家藥監(jiān)局批準(zhǔn)蘇州阿格斯醫(yī)療技術(shù)有限公司生產(chǎn)的創(chuàng)新產(chǎn)品“一次性使用血管內(nèi)成像導(dǎo)管”注冊申請���。該產(chǎn)品需配合光學(xué)干涉斷層成像系統(tǒng)使用,用于在醫(yī)療機(jī)構(gòu)中對需要進(jìn)行腔內(nèi)介入治療患者的冠狀動脈成像���。
2.國家藥監(jiān)局通過優(yōu)先審評審批程序附條件批準(zhǔn)榮昌生物制藥(煙臺)股份有限公司申報(bào)的治療用生物制品注射用泰它西普(商品名:泰愛)上市�����。該藥為我國自主研發(fā)的創(chuàng)新藥�,與常規(guī)治療聯(lián)合����,適用于在常規(guī)治療基礎(chǔ)上仍具有高疾病活動的活動性、自身抗體陽性的系統(tǒng)性紅斑狼瘡(SLE)成年患者����。
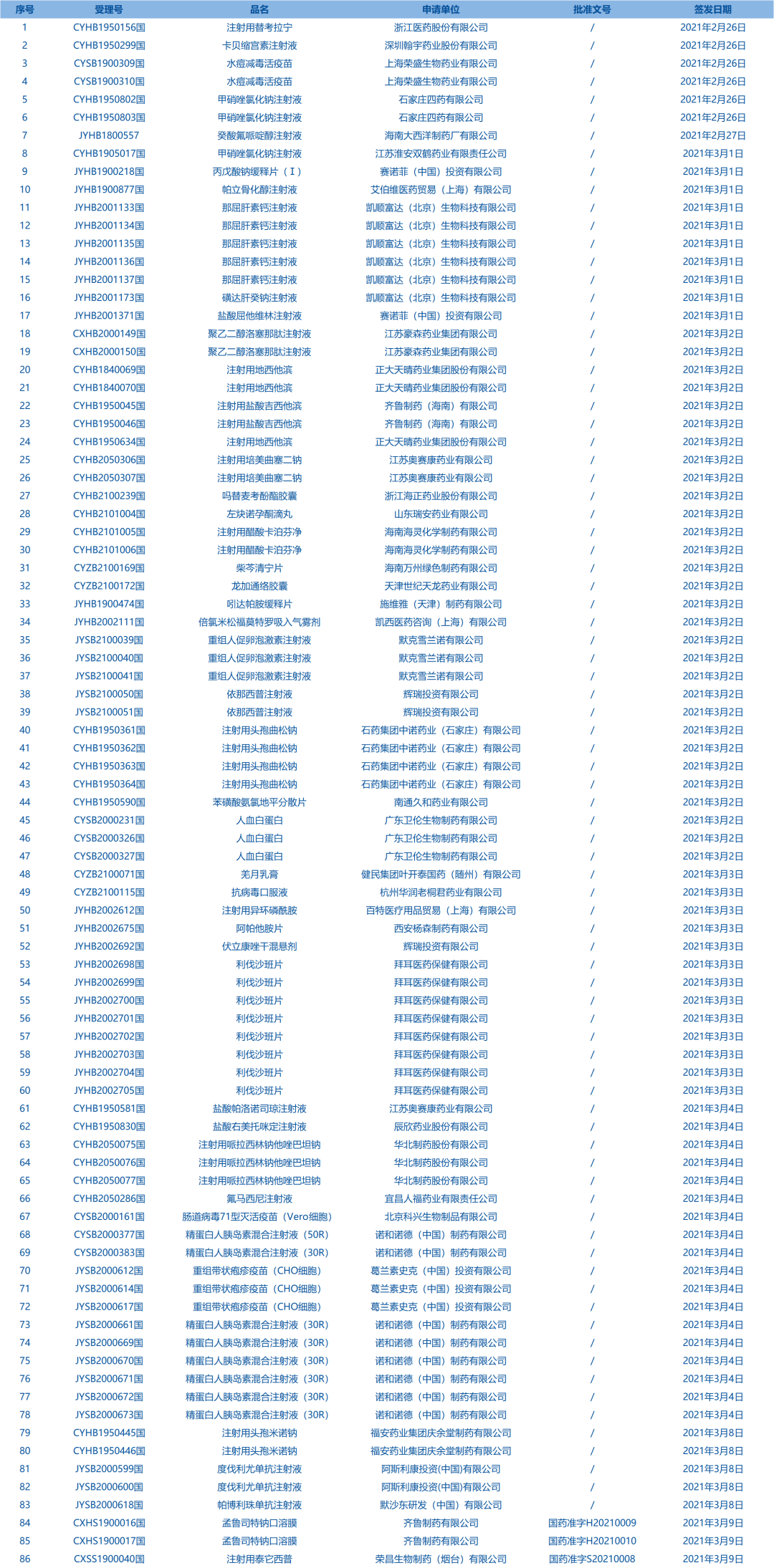
3.國家藥監(jiān)局發(fā)布3期藥品批準(zhǔn)證明文件待領(lǐng)信息,共包括106個受理號����,涉及浙江醫(yī)藥股份有限公司等企業(yè)�����。(截至3月14日)

4.國家藥監(jiān)局發(fā)布6期醫(yī)療器械批準(zhǔn)證明文件(準(zhǔn)產(chǎn))待領(lǐng)信息���,共包括72個受理號,涉及先健科技(深圳)有限公司等企業(yè)�����。(截至3月14日)

5.CDE網(wǎng)站公示15個仿制藥一致性評價(jià)任務(wù)��,涉及丙氨酰谷氨酰胺注射液等藥品��。(截至3月13日)

6.CDE承辦受理29個新藥上市申請���,包括康柏西普眼用注射液等藥品�����。(截至3月13日)

醫(yī)藥企業(yè)觀察
1.深圳信立泰藥業(yè)股份有限公司發(fā)布公告稱����,公司非公開發(fā)行不超過7,000萬股新股的申請獲得中國證監(jiān)會核準(zhǔn)批復(fù)。
2.石藥集團(tuán)全資附屬公司上海津曼特生物科技有限公司與康諾亞生物醫(yī)藥科技有限公司訂立協(xié)議�����,津曼特生物將獲得康諾亞生物授出的CM310(一種抗IL-4Rα的重組人源化單抗)在中國大陸地區(qū)針對中重度哮喘和慢性阻塞性肺病(COPD)等呼吸系統(tǒng)疾病開發(fā)及商業(yè)化的獨(dú)家權(quán)利����。
3.浙江昂利康制藥股份有限公司首次通過股份回購專用證券賬戶以集中競價(jià)方式實(shí)施回購股份,回購股份數(shù)量210,000股�,占公司總股本的0.22%,最高成交價(jià)為33.34元/股����,最低成交價(jià)為32.45元/股�,成交總金額6,919,443元。
4.蘇州貝康醫(yī)療股份有限公司與蘇州BioX生命智能產(chǎn)業(yè)研究院訂立研究成果轉(zhuǎn)化合作協(xié)議��。根據(jù)合作協(xié)議����,蘇州BioX同意就遺傳病診斷及遺傳咨詢的人工智能技術(shù)應(yīng)用提供學(xué)術(shù)研究服務(wù),而貝康醫(yī)療同意基于蘇州BioX的學(xué)術(shù)研究成果及知識產(chǎn)權(quán)�����,利用自身豐富的行業(yè)經(jīng)驗(yàn)提供產(chǎn)品開發(fā)服務(wù)。
5.海思科醫(yī)藥集團(tuán)股份有限公司控股子公司FT集團(tuán)擬與美國風(fēng)投公司ForesiteCapital設(shè)立的非上市公司FL2021-001,Inc.簽署交易協(xié)議���,將其全資子公司FT控股之全部股權(quán)轉(zhuǎn)讓給FL2021-001,Inc.���。FT 控股及其全資子公司 FronThera U.S. Pharmaceuticals LLC除仍擁有在研項(xiàng)目TYK2產(chǎn)品外,所有非TYK2產(chǎn)品的在研項(xiàng)目所屬專利和權(quán)益等將轉(zhuǎn)給海思科��,涉及到Autotaxin�、THR-β、Ask1��、Nrf2����、hemoglobin modifier 等。
藥械集中采購
1.上海陽光醫(yī)藥采購網(wǎng)發(fā)布通知�����,公布一批新增醫(yī)保談判藥品信息�,并就掛網(wǎng)工作進(jìn)行安排。通知明確���,本次掛網(wǎng)的藥品信息于3月11日正式生效�����,共包括蒺藜皂苷膠囊等26個藥品�����,涉及長白山制藥股份有限公司等企業(yè)�。
2.河北省醫(yī)保局等七部門聯(lián)合印發(fā)《推動藥品集中帶量采購工作常態(tài)化制度化開展實(shí)施方案》,該方案明確對于國家組織帶量采購范圍外的藥品�����,河北省將獨(dú)立開展��,或與京津���,或與福建三明聯(lián)合開展集中帶量采購,同時(shí)鼓勵市級統(tǒng)籌區(qū)有序開展集中帶量采購�。
3.浙江省藥械采購中心發(fā)布關(guān)于再次提醒提交醫(yī)藥企業(yè)價(jià)格和營銷行為信用承諾書的通知,對于未提交書面承諾的企業(yè)�,自4月1日起,不再接受其新的投標(biāo)或掛網(wǎng)申請��;自6月1日起�,對已中標(biāo)或掛網(wǎng)的醫(yī)藥企業(yè)及其產(chǎn)品�,在保障臨床需求的前提下撤銷其掛網(wǎng)����。
文章來源:中國醫(yī)藥報(bào)