醫(yī)藥 · 看點
《化妝品注冊備案資料管理規(guī)定》及《化妝品新原料注冊備案資料管理規(guī)定》發(fā)布��,曲馬多注射劑和單方口服劑說明書修訂……3月1日~3月7日����,醫(yī)藥行業(yè)的這些事情值得關(guān)注���。
行業(yè) · 政策動態(tài)
1.十三屆全國人大四次會議在京開幕,國務(wù)院總理李克強向大會作政府工作報告�。在部署2021年重點工作時,政府工作報告指出���,做好今年工作�����,要更好統(tǒng)籌疫情防控和經(jīng)濟社會發(fā)展�。堅持常態(tài)化防控和局部應(yīng)急處置有機結(jié)合��,繼續(xù)毫不放松做好外防輸入�、內(nèi)防反彈工作,抓好重點區(qū)域和關(guān)鍵環(huán)節(jié)防控����,補上短板漏洞,嚴防出現(xiàn)聚集性疫情和散發(fā)病例傳播擴散����,有序推進疫苗研制和免費接種,提高科學(xué)精準防控能力和水平�。
政府工作報告提出���,推進衛(wèi)生健康體系建設(shè)。持續(xù)推進健康中國行動�����,深入開展愛國衛(wèi)生運動����,深化疾病預(yù)防控制體系改革����,創(chuàng)新醫(yī)防協(xié)同機制,健全公共衛(wèi)生應(yīng)急處置和物資保障體系�,建立穩(wěn)定的公共衛(wèi)生事業(yè)投入機制。深化公立醫(yī)院綜合改革�����,擴大國家醫(yī)學(xué)中心和區(qū)域醫(yī)療中心建設(shè)試點�����,加強全科醫(yī)生和鄉(xiāng)村醫(yī)生隊伍建設(shè)����,提升縣級醫(yī)療服務(wù)能力����,加快建設(shè)分級診療體系����。
政府工作報告明確,堅持中西醫(yī)并重��,實施中醫(yī)藥振興發(fā)展重大工程�。支持社會辦醫(yī),促進“互聯(lián)網(wǎng)+醫(yī)療健康”規(guī)范發(fā)展�。強化食品藥品疫苗監(jiān)管。優(yōu)化預(yù)約診療等便民措施�,努力讓大病�����、急難病患者盡早得到治療��。
政府工作報告表示�,居民醫(yī)保和基本公共衛(wèi)生服務(wù)經(jīng)費人均財政補助標準分別再增加30元和5元,推動基本醫(yī)保省級統(tǒng)籌�、門診費用跨省直接結(jié)算�。建立健全門診共濟保障機制���,逐步將門診費用納入統(tǒng)籌基金報銷�,完善短缺藥品保供穩(wěn)價機制�����,采取把更多慢性病、常見病藥品和高值醫(yī)用耗材納入集中帶量采購等辦法�,進一步明顯降低患者醫(yī)藥負擔(dān)。
2.國家藥品監(jiān)督管理局發(fā)布《化妝品注冊備案資料管理規(guī)定》《化妝品新原料注冊備案資料管理規(guī)定》��,以貫徹落實《化妝品注冊備案管理辦法》�,規(guī)范指導(dǎo)化妝品��、化妝品新原料注冊與備案工作���。兩個規(guī)定自2021年5月1日起施行�����。
3.國家藥監(jiān)局發(fā)布公告���,明確化妝品注冊備案信息服務(wù)平臺啟用�����,原注冊備案平臺已注冊和備案產(chǎn)品資料轉(zhuǎn)移���,化妝品原料安全相關(guān)信息報送,祛斑美白和防脫發(fā)化妝品功效評價檢驗報告����,普通化妝品年度報告等《化妝品注冊備案資料管理規(guī)定》實施事宜。
4.國家藥監(jiān)局發(fā)布《化妝品中防腐劑檢驗方法》《化妝品中硼酸和硼酸鹽檢驗方法》《化妝品中對苯二胺等32種組分檢驗方法》《化妝品中維甲酸等8種組分檢驗方法》《體外哺乳動物細胞微核試驗》《化妝品祛斑美白功效測試方法》《化妝品防脫發(fā)功效測試方法》7個文件�����,作為《化妝品安全技術(shù)規(guī)范(2015年版)》修訂或新增的檢驗方法�,納入相應(yīng)章節(jié)���。
5.國家藥監(jiān)局發(fā)布仿制藥參比制劑目錄(第三十九批)��,涉及匹維溴銨片等藥品�����。
6.國家藥監(jiān)局修訂曲馬多注射劑和單方口服劑說明書�����,本品的上市許可持有人應(yīng)依據(jù)有關(guān)規(guī)定����,按照說明書修訂要求,提出修訂說明書的補充申請�,于5月24日前報國家藥監(jiān)局藥審中心(CDE)或省級藥品監(jiān)管部門備案。
7.國家藥監(jiān)局公開征求《醫(yī)療器械應(yīng)急審批程序(修訂稿征求意見稿)》意見��,征求意見截止時間為4月15日����。
8.國家藥監(jiān)局器審中心已啟動《無創(chuàng)血糖/葡萄糖監(jiān)測產(chǎn)品注冊技術(shù)審查指導(dǎo)原則》的編制工作����,并就指導(dǎo)原則的制定工作征集有相關(guān)工作經(jīng)驗的境內(nèi)外制造商及其他相關(guān)單位信息。
產(chǎn)品研發(fā) · 上市信息
1. 國家藥監(jiān)局通過特別審批程序應(yīng)急批準中國中醫(yī)科學(xué)院中醫(yī)臨床基礎(chǔ)醫(yī)學(xué)研究所的清肺排毒顆粒���、廣東一方制藥有限公司的化濕敗毒顆粒��、山東步長制藥股份有限公司的宣肺敗毒顆粒上市�����。
2. 國家藥監(jiān)局通過優(yōu)先審評審批程序附條件批準上海艾力斯醫(yī)藥科技股份有限公司申報的1類創(chuàng)新藥甲磺酸伏美替尼片(商品名:艾弗沙)上市���。該藥為我國自主研發(fā)并擁有自主知識產(chǎn)權(quán)的創(chuàng)新藥��,適用于既往經(jīng)表皮生長因子受體(EGFR)酪氨酸激酶抑制劑(TKI)治療時或治療后出現(xiàn)疾病進展�,并且經(jīng)檢測確認存在EGFR T790M突變陽性的局部晚期或轉(zhuǎn)移性非小細胞性肺癌(NSCLC)成人患者的治療����。
3.國家藥監(jiān)局發(fā)布各省醫(yī)療器械許可備案相關(guān)信息(截至2021年2月28日)。

4.國家藥監(jiān)局發(fā)布3期藥品批準證明文件待領(lǐng)信息/藥品通知件待領(lǐng)取信息����,共包括72個受理號,涉及仙琚制藥股份有限公司等企業(yè)�。(截至3月5日)

5.國家藥監(jiān)局發(fā)布4期醫(yī)療器械批準證明文件(準產(chǎn))待領(lǐng)信息,共包括57個受理號���,涉及北京惠中醫(yī)療器械有限公司等企業(yè)����。(截至3月5日)

6. CDE承辦受理11個新藥上市申請,包括羅沙司他膠囊等藥品��。(截至3月5日)

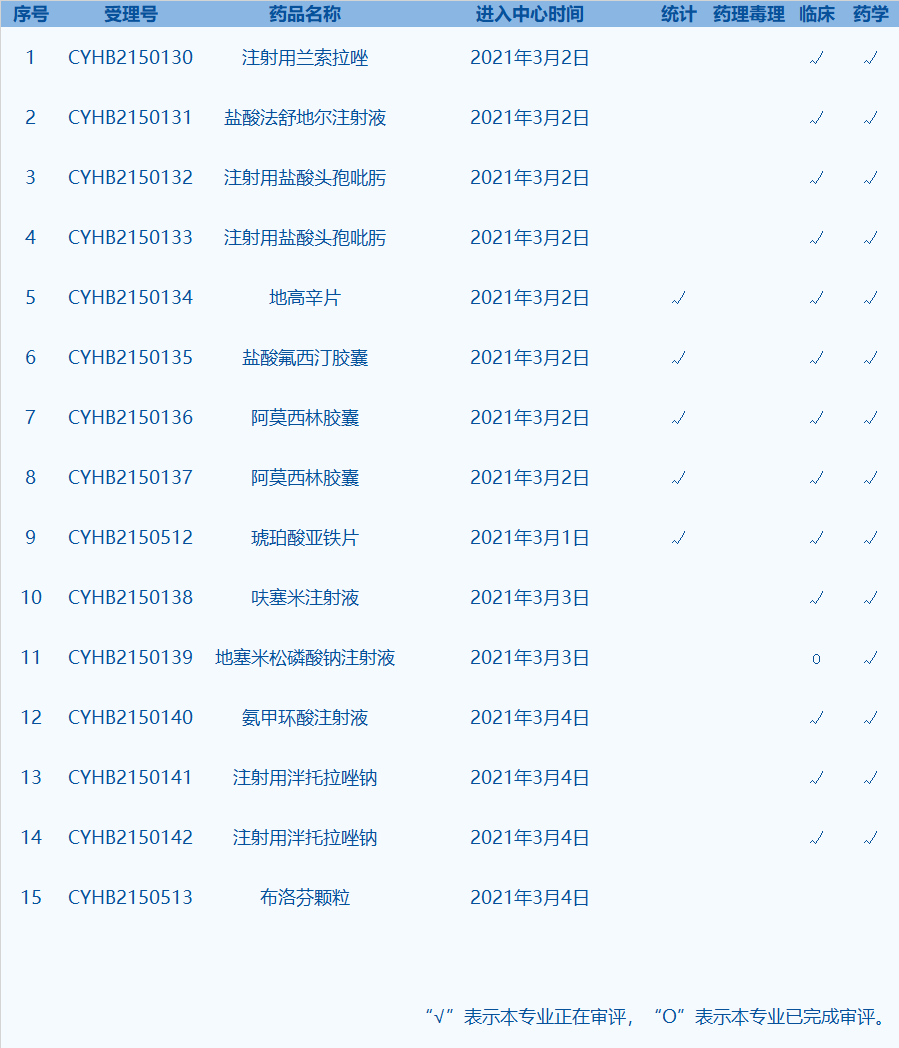
7. CDE網(wǎng)站公示15個仿制藥一致性評價任務(wù)�,涉及地高辛片等藥品���。(截至3月5日)
8.CDE網(wǎng)站信息顯示��,上海濟煜醫(yī)藥科技有限公司申請的磷酸索尼德吉膠囊擬進入優(yōu)先審評審批程序����。(截至3月7日)

醫(yī)藥企業(yè)觀察
1.英科醫(yī)療全資子公司安徽英科醫(yī)療用品有限公司擬投資50億元人民幣投資英科醫(yī)療產(chǎn)業(yè)園年產(chǎn)520億只(5200萬箱)高端醫(yī)用手套項目��。
2.李氏大藥廠宣布公司全資附屬公司兆科藥業(yè)(兆科合肥)與昆藥集團股份有限公司的全資附屬公司昆明貝克諾頓藥品銷售有限公司(KBNS)已簽訂產(chǎn)品銷售服務(wù)協(xié)議�����,據(jù)此�����,兆科合肥向KBNS授出磺達肝癸鈉注射液于中國指定區(qū)域的獨家推廣權(quán)����。
3.科技公司默克中國與廣州醫(yī)藥集團有限公司在廣州簽署戰(zhàn)略合作備忘錄。雙方將依托粵港澳大灣區(qū)在生物醫(yī)藥建設(shè)領(lǐng)域的發(fā)展優(yōu)勢和開放機遇��,在業(yè)務(wù)模式創(chuàng)新��、產(chǎn)品研發(fā)以及市場拓展等方面進行深入探索與合作��。
4.萊美藥業(yè)宣布向公司控股股東中恒集團及其一致行動人中恒同德和廣投國宏定向發(fā)行股票約2.44億股����,發(fā)行價格為4.45元/股,實際募集資金總額為10.84億元���,定向增發(fā)后���,發(fā)行對象的股票數(shù)量合計占萊美藥業(yè)總股本的比例將超過30%。
5.復(fù)旦兒科醫(yī)院�、上海復(fù)星醫(yī)療、邁勝醫(yī)療科技集團三方合作簽約����,致力于在兒童腫瘤質(zhì)子治療、科研合作��、人才培養(yǎng)等方面建立全面戰(zhàn)略合作�����。
藥品集中采購
1.天津市醫(yī)藥采購中心正式發(fā)布通知,為做好京津冀藥品聯(lián)合帶量采購工作����,開始進行相關(guān)藥品采購數(shù)據(jù)填報工作��,填報內(nèi)容為本單位京津冀藥品聯(lián)合帶量采購相關(guān)藥品2019年和2020年采購數(shù)據(jù)�,包括總采購量、最低有效采購價���、最低有效采購價對應(yīng)采購量等��,同時填報未來一年需求量�����。填報時間為3月3日至3月12日�����。
2.上海陽光醫(yī)藥采購網(wǎng)發(fā)布《關(guān)于開展第四批全國藥品集中采購上海地區(qū)中選藥品掛網(wǎng)工作的通知》,明確自3月4日起����,申報企業(yè)可登錄“上海市醫(yī)藥采購服務(wù)與監(jiān)管信息系統(tǒng)”上報上海地區(qū)中選藥品相關(guān)信息�����,申報截止時間為3月12日�����。
3.河北省發(fā)布通知����,將開展一次性使用輸液器類���、靜脈留置針類兩類低值醫(yī)用耗材帶量采購�����。通知明確����,非中選產(chǎn)品全部納入河北省醫(yī)用藥品器械采購中心監(jiān)控管理�����,納入監(jiān)控目錄的非中選產(chǎn)品的采購量不得高于中選產(chǎn)品的最低采購量,監(jiān)測發(fā)現(xiàn)高于中選產(chǎn)品的最低采購量�,將暫停該非中選產(chǎn)品采購。
文章來源:中國醫(yī)藥報